|
中国临床试验登记数据一览
随着中国医药政策变革逐步深入,当前的中国医药行业也慢慢出现成果涌现的节奏。笔者通过对药物临床试验登记与信息公示平台(chinadrugtrials.org.cn)的所有数据进行统计分析,试图一览当前中国药物临床试验的登记的情况。
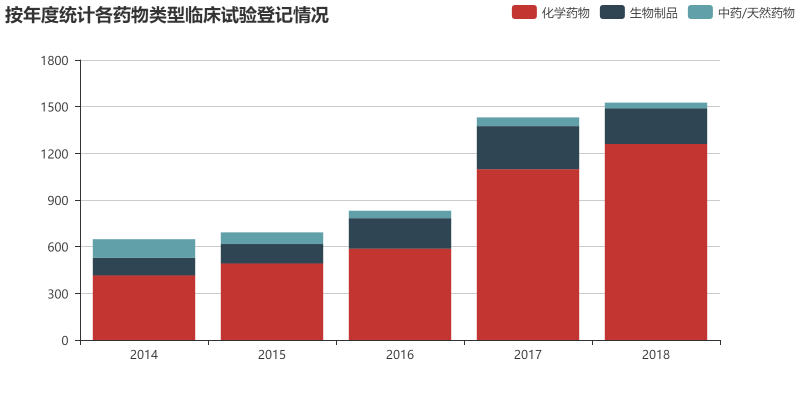
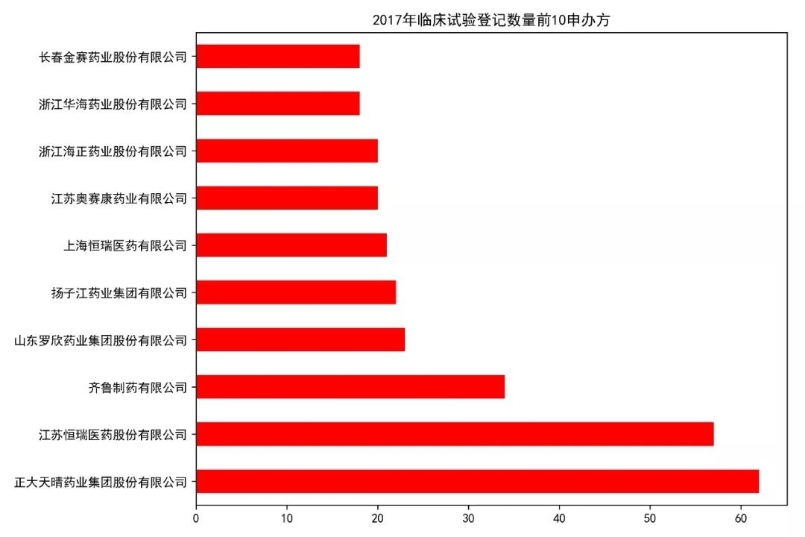
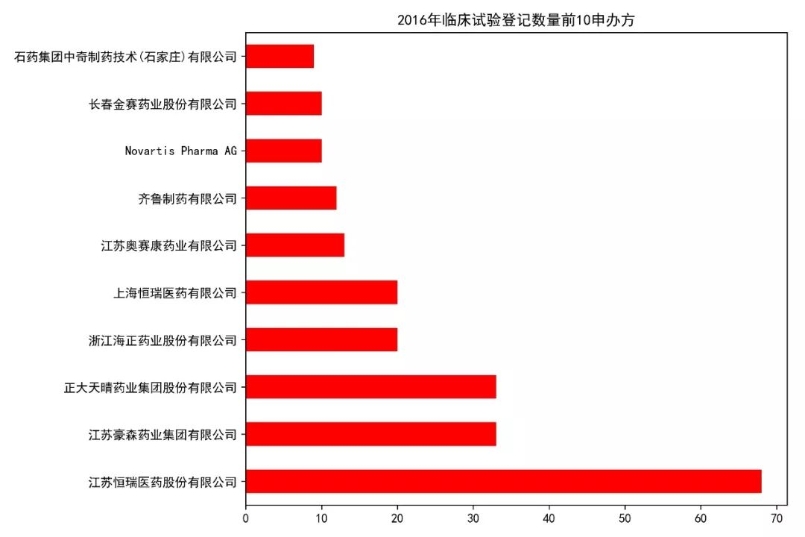
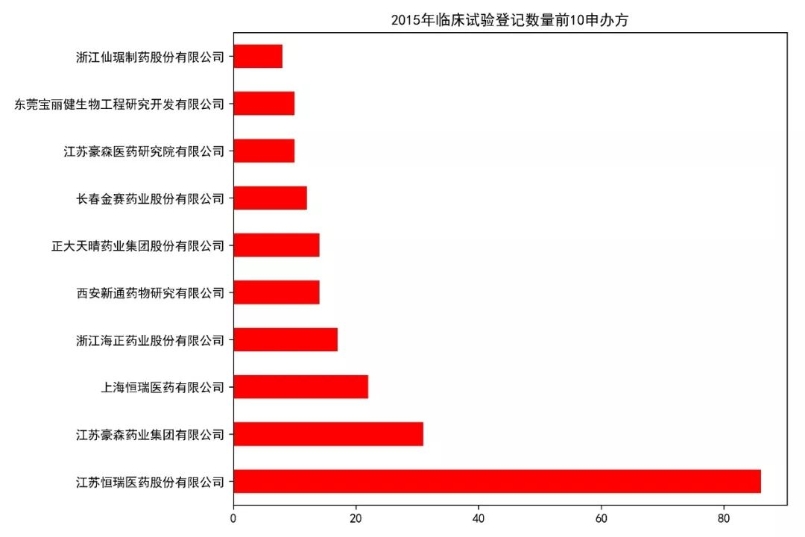
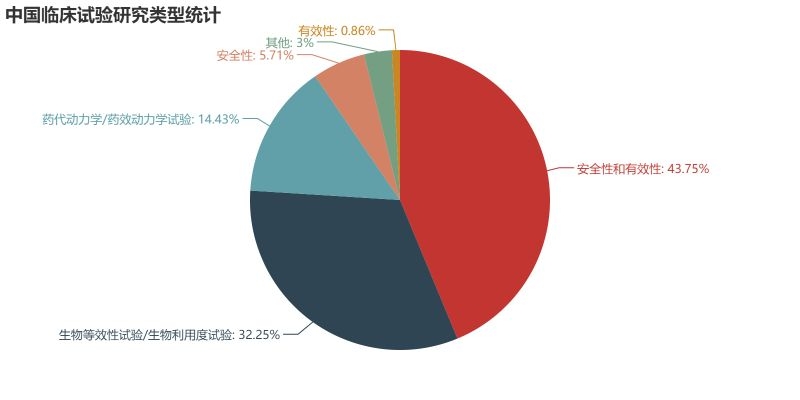
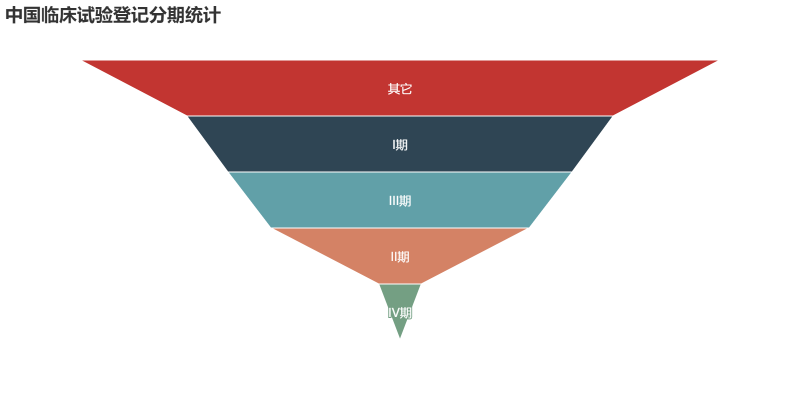
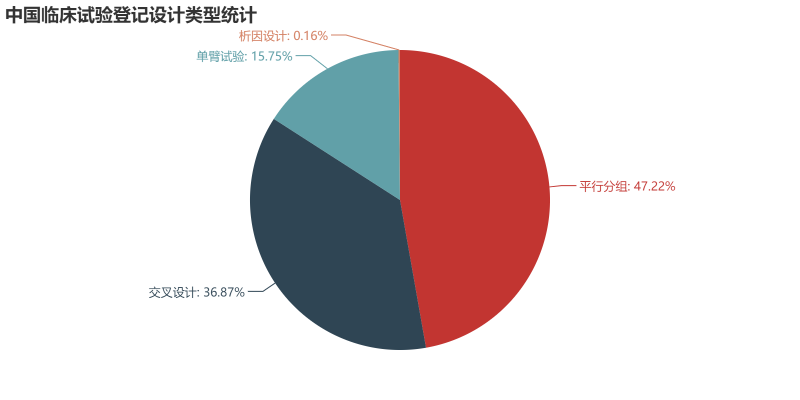
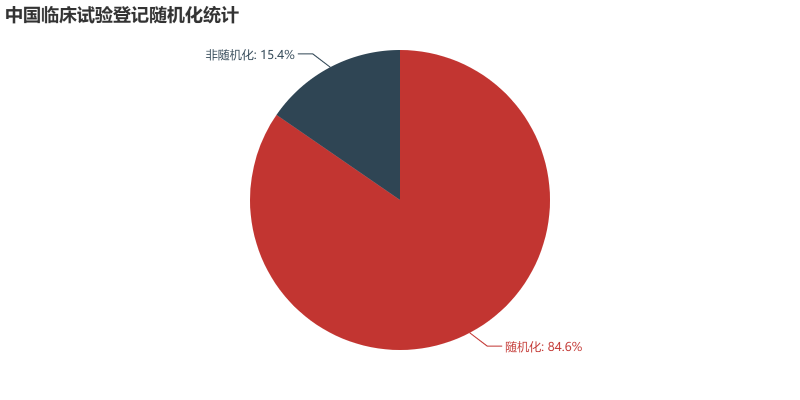
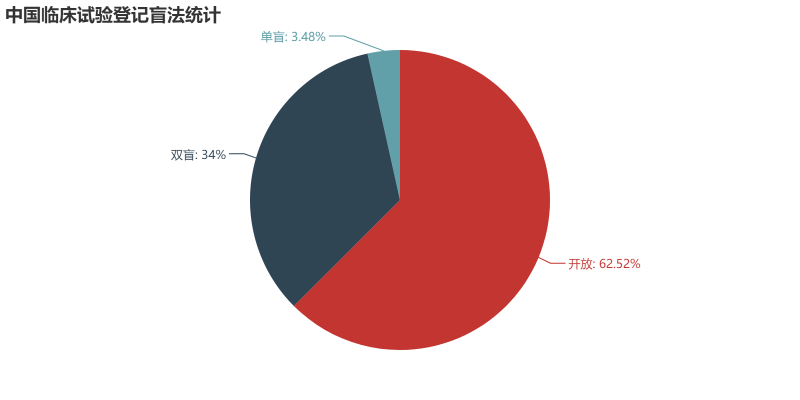
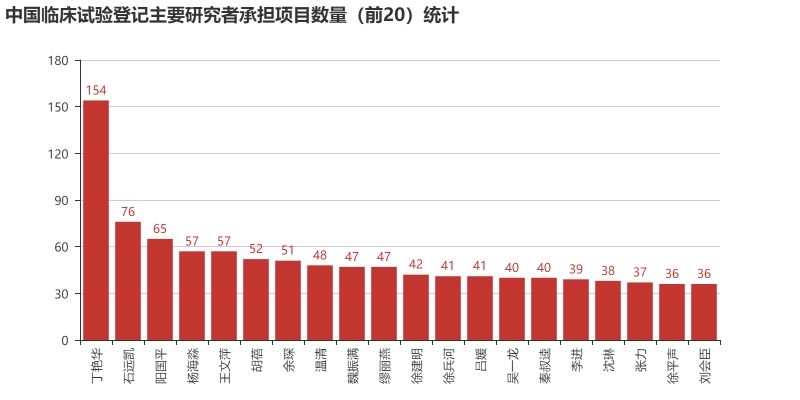
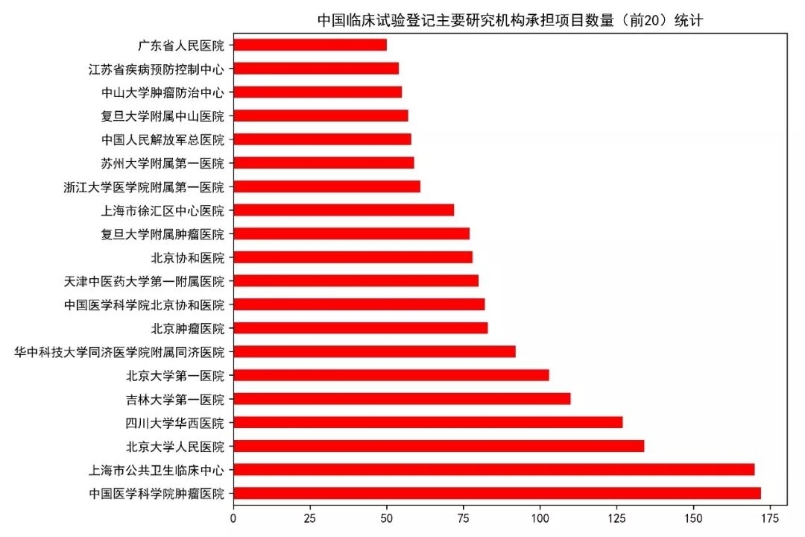
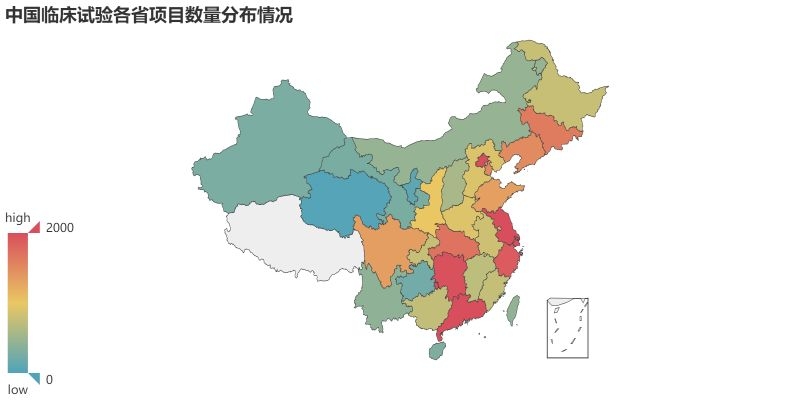
试验药物分析 首先我们来看目前登记的临床试验中,试验药物的类型分布情况。从数据来看,试验药物分为化学药物(4708例)、生物制品(1138例)、中药/天然药物(664例)。化学药物在国内最先起步,另外加上一致性评价的深入,占据了所有试验中的72.32%。生物制品紧随其后,相信随着一众抗体新药和生物类似物的推进,生物制品的占比会逐步提升。作为中药大国,中药/天然药物的临床试验如此之少,应该引起所有从业者的深思。 我们进一步分析各类型药物从2014-2018年的数量变化情况。整体来看,临床试验数量从2017有一个大的提升,从化学药的数量提升幅度来看,这应该是仿制药一致性评价释放的临床需求。生物制品的数量每年也有一个稳步的提升,因为2018年还未结束,这里还无法预知2018年整年的情况。在国家大力推进中药产业的背景下,中药/天然药物则呈现出逐年减少的趋势。这说明当前的医药审批政策变革其实给每个中药研发企业提出了新的挑战,未来如何应对,还需要进一步探索。但可以肯定的是,大样本的临床试验是证明药物安全有效的有力证据,未来还是应该从这方面下功夫。 申办方分析 我们对平台上登记的所有临床试验的申办方进行统计排名,临床试验登记数量前20的申办方如图所示。某些情况下,同一临床试验会有多个申办方,我们这里对其进行分拆,作为单一申办方进行统计。从结果来看,江苏恒瑞医药股份有限公司共有351个临床项目,远远领先于国内其他公司,恒瑞作为国内医药公司的一哥可谓是名副其实。正大天晴以162个临床项目位列第二,豪森(134)、海正(98)、齐鲁(97)紧随其后,这些公司倍受同行关注,从这一数据来看确实是有原因的。 对每一年的申办方排名情况进行汇总如下,这里不再逐一分析。恒瑞从14年到18年每年都能保持50项以上临床试验登记,真是让人不得不佩服恒瑞对于研发的投入力度和管线的布局能力。 试验设计分析 对申办方登记的试验分类信息进行分析,当前的国内的临床试验主要分为安全性和有效性(2995项)、生物等效性试验/生物利用度试验(2208)、药代动力学/药效动力学试验(988)、安全性(391)、有效性(59)、其他(205)。生物等效性试验/生物利用试验可以被简单认为是一致性评价试验,在所有试验中占到了32.25%,可见当前一致性评价的紧迫性。 我们再对中国临床试验按照分期进行统计,结果如图。平台登记的分期信息主要分为五类:其它(2560项,主要是一致性评价项目)、I期(1705项)、III期(1377项)、II期(1033项)、IV期(171项)。I期项目数量排在第二位,可以说明当前中国医药企业的前期研发越来越多地转向了临床试验阶段。III期项目达到1377项,希望未来我们可以看到其中的产品被临床试验证明,进而早日上市。 我们另外简要统计了临床试验设计类型、随机化、盲法的情况,这里不再展开,大家可以看图了解。 主要研究者分析 临床试验的开展离不开研究者的鼎力支持,我们接下来对所有项目的主要研究者进行统计。主要研究者承担项目数量排名前20的如图所示,每一位研究者在各自领域内都是大名鼎鼎。 对主要研究机构承担的项目数量进行统计,其排名基本上与主要研究者所在单位相匹配。有意思的是,前20名机构中,大部分都是各大学的附属医院,这说明在科学研究上,学术机构还是走在了前列。 最后我们统计了各机构所承担的临床项目数量按照其所在省份分布的情况,由于登记信息千差万别,这里我们对数据只是进行了简单的清洗整理,但在分布规律上应该不会出现偏差。 总结 通过以上简单的分析,我们可以看出当前国内的临床试验呈现出良好的增长态势,除了一致性评价带来的迅速增长外,国内创新药企业的研发阶段逐步向临床阶段转移也作出了一定贡献。I期临床数量作为基石,预示着未来II、III期临床数量的增长。在临床试验区域分布方面,著名医学院校所在省份承担了国内大量的临床项目,医学院校的科研能力和影响力还是得到了众多申办方的认可。 本文只是通过简单的统计分析对临床试验情况进行直观的描述,如有不妥之处,欢迎留言讨论。另外,如果大家想了解其他维度的信息,也欢迎大家留言,笔者后面会进一步深入分析。